导读:细胞死亡途径是抗肿瘤化疗的重要药物靶点。
11月2日,中国科学院大学钱友存团队在期刊《Cell Reports》上在线发表题为“Triggering endogenous Z-RNA sensing for anti-tumor therapy through ZBP1-dependent necroptosis”的研究论文,研究证明,氧化应激诱导的Z-RNA直接促进肿瘤细胞坏死性细胞凋亡,从而抑制肿瘤生长。因此,通过诱导肿瘤中的氧化应激可能有助于促进基于Z-RNA驱动的坏死性细胞凋亡的癌症治疗,具有潜在的治疗策略。

https://www.cell.com/cell-reports/fulltext/S2211-1247(23)01389-X
研究背景
01
细胞死亡途径是抗肿瘤化疗的重要药物靶点。例如,化疗药物顺铂可以诱导肿瘤细胞凋亡,从而控制肿瘤的生长。坏死性细胞死亡(necroptosis)作为一种非caspase依赖的程序性细胞死亡形式,最近据报道在一些接受化疗药物处理的肿瘤细胞系中发生。然而,大多数有关肿瘤细胞坏死性细胞死亡的研究都是基于体外实验进行的,因此在体内诱导肿瘤坏死性细胞死亡的有效性仍需要更多的调查。虽然一些过程,例如肿瘤坏死因子(TNF)/ TNF受体(TNFR)信号通路的参与或缺氧的产生已被揭示以解释该效应,但对坏死性细胞死亡机制的更好理解仍对肿瘤治疗的发展至关重要。
压力颗粒(SGs)是一种非膜结构的细胞质小体,在多种压力条件下,如氧化应激,聚集阻滞的翻译起始复合物,包括mRNA和大量RNA结合蛋白。由于压力颗粒(SGs)具有动态特性和复杂的RNA-蛋白相互作用,受不同触发器诱导形成的压力颗粒可能具有不同的功能。根据与压力颗粒相关蛋白的作用,普遍认为压力颗粒参与了多种疾病的病理过程,例如神经退行性疾病和癌症。然而,压力颗粒对疾病发病机制的影响的分子机制尚不明确。
研究发现
02
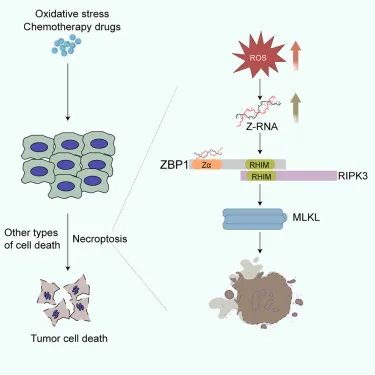
在研究中,研究人员报告了氧化应激强烈诱导宿主细胞内源性Z-RNA的形成,然后这些Z-RNA定位到压力颗粒中,通过直接被ZBP1感知来触发坏死性细胞死亡。氧化应激显著增加了肿瘤细胞中Z-RNA的水平,然后这些Z-RNA通过ZBP1直接触发肿瘤细胞坏死性细胞死亡。诱导的Z-RNA定位到压力颗粒对ZBP1的感知至关重要。氧化应激诱导的Z-RNA通过ZBP1介导的坏死性细胞死亡显著促进肿瘤化疗效果。因此,研究确定了氧化应激作为促进Z-RNA形成的关键触发因子,并展示了Z-RNA如何通过ZBP1直接感知来触发抗肿瘤的坏死性细胞死亡。
恢复氧化应激诱导的坏死性凋亡
促进了人类肿瘤细胞的化疗效果
03
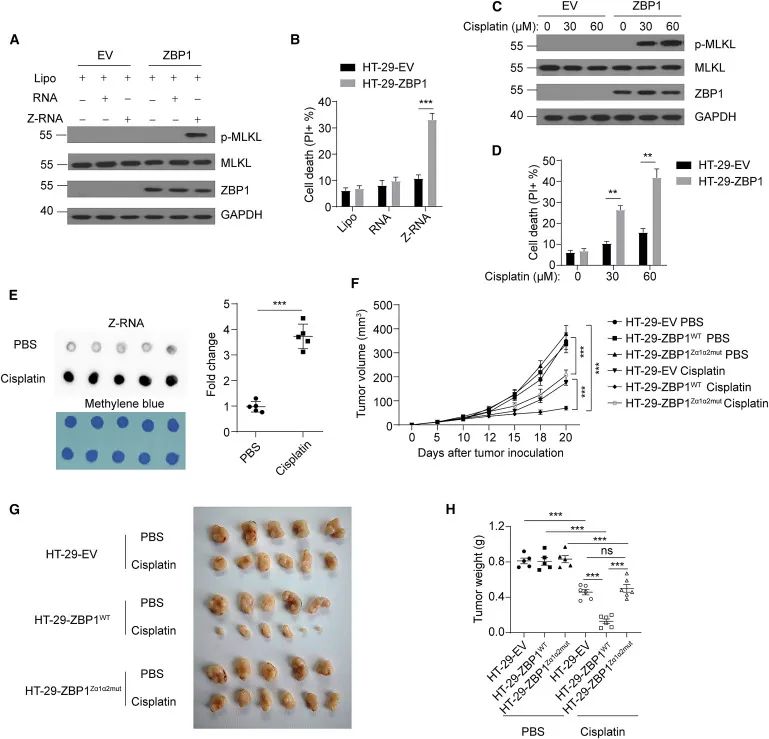
由于HT-29细胞中RIPK3和MLKL的表达正常,研究人员恢复了肿瘤细胞中的ZBP1表达,并转染了亚砷酸盐诱导的Z-RNAs,这强烈地触发了恢复的细胞中的坏死程序性细胞死亡。顺铂在具有外源ZBP1表达的HT-29细胞中显著诱导了坏死程序性细胞死亡。接着,研究人员检查了顺铂是否能够在人类肿瘤体内诱导Z-RNA水平的增加。与亚砷酸盐的效果类似,顺铂治疗显著增加了HT-29肿瘤中的Z-RNA水平,表明顺铂可以诱导氧化应激以增加Z-RNA的产生。接着,研究人员研究了体内诱导的Z-RNAs的效应。研究人员观察到,尽管顺铂治疗仍然减小了HT-29肿瘤的大小和重量,这可能是由于细胞凋亡所致,但在HT-29肿瘤细胞中恢复外源WT而不是Zα突变的ZBP1进一步增强了顺铂对肿瘤生长抑制的治疗效果。
研究表明,促进氧化应激的治疗药物(如顺铂)可以诱导肿瘤中的Z-RNA产生,但人类肿瘤细胞可以通过调控ZBP1的表达来逃避Z-RNA引起的坏死程序性细胞死亡。同时,为了检查人类结直肠癌(CRC)组织中ZBP1的表达情况,研究人员使用两个不同的数据集从基因表达杂志库(GEO)中挖掘了内镜获取的肠黏膜腺瘤和来自同一患者正常黏膜的数据。总体而言,研究人员发现肿瘤细胞中ZBP1的表达水平降低。因此,通过外源表达ZBP1基因来治疗肿瘤细胞,可能会促进氧化应激诱导药物的化疗效果,或者与氧化应激试剂联合使用。这为开发基于ZBP1基因治疗的新型抗癌疗法提供了思路。
研究结果
04
综上所述,研究证明,氧化应激诱导的Z-RNA直接促进肿瘤细胞坏死性细胞凋亡,从而抑制肿瘤生长。因此,通过诱导肿瘤中的氧化应激可能有助于促进基于Z-RNA驱动的坏死性细胞凋亡的癌症治疗,具有潜在的治疗策略。
参考资料:
https://www.cell.com/cell-reports/fulltext/S2211-1247(23)01389-X
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。

