2023年12月14日,复旦大学附属中山医院樊嘉院士团队与上海科技大学张力烨团队及上海顿慧医疗合作,于Cell Press细胞出版社旗下期刊Cancer Cell在线发表了题为“Integrated multi-omics profiling to dissect the spatiotemporal evolution of metastatic hepatocellular carcinoma”的研究成果。本研究基于多组学平台,在国际上首次系统刻画了肝癌转移的时空演进全景图谱,揭示了肝癌转移的复杂进化轨迹和克隆选择机制,为研发肝癌转移预测的新标志物和治疗新靶点提供了宝贵的数据和理论基础。
肝细胞癌(简称“肝癌”)是世界上最常见的恶性肿瘤之一,在我国尤为高发,每年新发病例和死亡病例均占全球近一半。手术切除是目前肝癌治疗的首选方式,但70-80%的肝癌病人确诊时已发生肿瘤播散转移,为中晚期肝癌,失去了手术机会;即使手术切除,肝癌术后5年转移复发率高达60-70%。肝癌的转移复发是影响病人长期生存的主要原因,它已成为进一步提高肝癌整体疗效的瓶颈。因此,全面深刻认识肝癌转移复发的内在机制,探索更有效的干预新策略,已成为进一步提高肝癌病人总体生存率的关键课题。
近年来已有研究通过大规模测序揭示了驱动肝癌发生的基因组及转录组特征,但针对肝癌转移肿瘤的组学研究却鲜有研究报道。目前肝癌转移肿瘤的基因突变和分子表达全景图谱仍极度缺乏,肝癌在转移过程中的克隆选择等演化规律尚不清晰,导致肝癌转移病灶的临床诊疗仍然缺乏足够的理论指导,这些科学问题亟待解决。
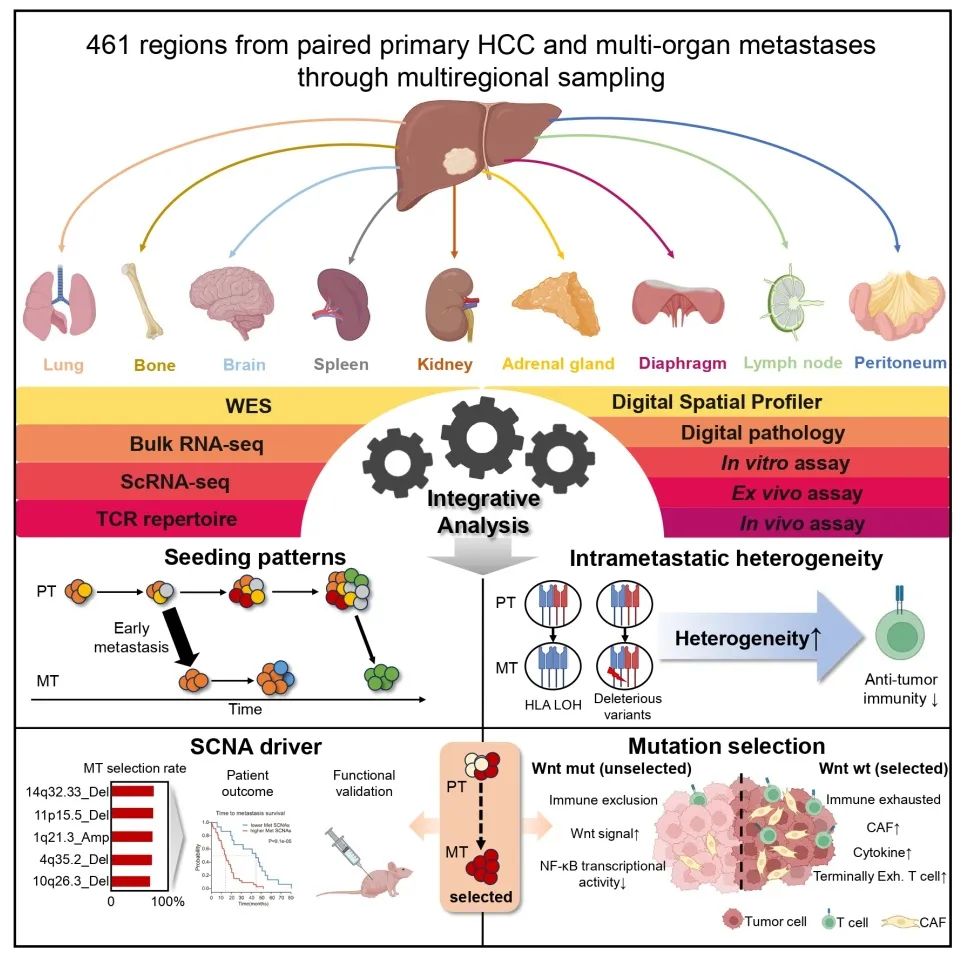
该研究整合时空多组学技术,通过原发转移配对样本的多区域取样联合多组学分析,绘制了肝癌转移过程的演化图谱,首次揭示了肝癌启动转移的分子时间,转移定植的克隆模式,转移肿瘤的瘤内异质性及其与微环境的相关性,驱动转移的关键事件,以及转移过程中克隆选择的机制,为肝癌转移的精准诊疗提供更深入的理论基础。
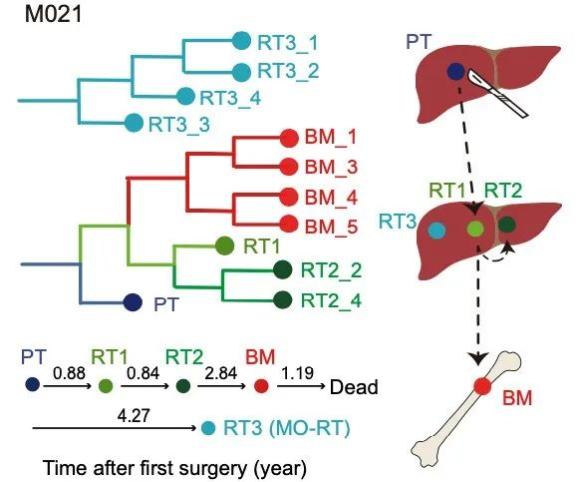
图1 一个出现转移患者多肿瘤基于基因组变异重构转移进化关系示意图。
复旦大学附属中山医院樊嘉院士、上海科技大学张力烨研究员、复旦大学附属中山医院孙云帆副研究员及上海顿慧医疗彭海翔博士为本文共同通讯作者,孙云帆副研究员、吴频博士、张泽凡博士、王泽健博士、周恺乾博士、宋敏芳博士、纪元教授、臧凤琳教授为本文共同第一作者。
该课题得到了国家自然科学基金、上海市创新集群等项目资助,顿慧医疗和上海科技大学超算中心为多组学数据产出和生物信息分析提供了大力支持。
作者专访
Cell Press细胞出版社公众号特别邀请樊嘉院士及其研究团队接受了专访,请他们为大家进一步详细解读。
CellPress:
肝癌的转移是影响病人长期生存的主要原因,那么肝癌转移的研究难点在哪里?
樊嘉院士:
不单单是肝癌,其实大多数的癌症转移都很难研究,难点在于:1. 采样难:从患者身上获取与肿瘤转移相关的组织样本对于临床研究至关重要,但这常常受到伦理和技术等多方面的限制。并且临床上大多数肝癌患者发现时都到了晚期,在这个阶段手术通常不是肝细胞癌患者,尤其是发生转移的晚期患者的标准治疗手段。2. 肝癌具有很高的肿瘤内以及不同个体肿瘤间异质性。多区域取样可以更全面准确地描述肿瘤内的亚克隆组成。此外获取配对的原发性肿瘤和转移灶病理样本很关键,因为非配对样本无法用来追踪肿瘤演化和揭示转移的规律。3. 转移是个高度复杂过程,其中肿瘤的基因组突变,表观遗传学变化,肿瘤与肿瘤微环境的互作都发挥了至关重要的作用。任何单一组学数据回答的问题都是有限,只有综合分析多种组学数据(比如说外显子测序;转录组测序;ATAC-Seq;单细胞测序;蛋白免疫组化染色等等)才能更全面地理解和找到转移过程中关键因素。所以在这个研究中,通过对来自两个独立的医疗中心,“ZSH-FD”(复旦大学附属中山医院)和“TMUCIH”(天津医科大学肿瘤医院)的2007-2021年的肝癌患者进行系统的收集、筛选,共有182名HCC患者被纳入了本课题,组织样本类型涉及原发性肿瘤、肝内复发性肿瘤,多种肝外器官转移肿瘤,以及配对的癌旁肝正常组织。大规模的数据集、配对的原发和转移样本、以及肿瘤的多区域多组学取样可以帮助我们更好的理解复杂的肝癌转移进程。
CellPress:
在您的研究中使用了多种生物信息学数据类型进行了多组学的整合分析,请问对于多组学分析您有什么分析建议?
张力烨研究员:
在我们的研究中,我们使用了全外显子组、转录组、单细胞转录组、空间转录组和数字病理等多种数据类型进行综合分析。进行多组学分析时,研究人员需要深入理解每种数据类型的独特特性和优势,同时探索这些不同数据之间的相互关联性。在分析的初始阶段,首先要确保数据的质量和可比性,仔细识别和校正可能影响数据分布的因素,例如批次效应以外的变异来源。对于那些特征数量远超过样本量的数据类型,可以利用特征提取等降维手段提取关键的特征,避免维数灾难。在探索不同数据类型之间的关联性时,我们特别关注于识别这些数据类型之间的共有特征和相互作用,因为这些关联性往往富含深刻的生物学意义,通常来说多维数据均支持的一些发现和猜想后续成功验证的几率会大大增加。例如,在我们的研究中,我们发现基于WES数据推测的具有转移选择倾向的Wnt野生型样本,在各种转录组数据中均富集了免疫抑制的信号,这一点在免疫组化染色结果中也得到了印证。类似的策略也帮助我们找到了在多克隆转移中关键的缺氧信号通路,以及转移过程中被选择的拷贝数变异片段中关键的基因。这种整合方法使我们能够从多个角度深入了解肿瘤的生物学特性,为癌症的治疗提供了更为全面和精确的生物标记物。此外,这种多维度的数据整合也为我们提供了对肿瘤微环境更加详细的认识,使我们能够更好地理解肿瘤细胞与周围微环境之间的复杂相互作用。
CellPress:
本研究您主要关注肝癌转移的演化规律,请具体介绍一下主要发现。
张力烨研究员:
与以往的研究不同,我们对肝癌患者配对的原发灶和转移灶均进行了多区域取样测序。多区域取样的策略使我们能够以前所未有的清晰度观察转移性肝细胞癌的基因组进化模式,并加深了我们对HCC转移进程中转移灶来源,克隆组成和转移时间的理解。
由于肝癌发病长见多病灶且多复发,而且在多原发灶和复发灶有很大频率的肿瘤具有不同的遗传来源。尽管数量较少,但我们的结果初步表明在同一患者,具有多个不同遗传来源的肿瘤,往往有且只有一个来源的肿瘤谱系可以进行远端器官转移播散。
在肝癌转移的克隆播散模式上,除了传统的单克隆转移,肝癌中也存在多克隆转移模式(多克隆转移指转移灶的组成非单次/单克隆的定植),并且多克隆转移模式的患者表现出更差的临床预后。
在这个研究中基于转移灶与原发灶突变相似度评估了转移时间,我们发现早期转移在肝癌患者中占主导地位,这使得转移灶与原发灶之间的共有的突变较少。同时早期转移也意味着肿瘤可能有更多时间在远端器官进行不断的克隆演化,我们还发现在肝癌异质性与在定植后所积累的抗原递呈相关突变高度相关。
早期转移,多克隆转移模式,定植后抗原递呈突变的积累这些演化规律一定程度解释了我们观察到的肝癌转移灶的高度异质性。我们最初很惊讶的发现配对的队列研究中发现肝癌转移灶的异质性并没有显著低于原发灶,不过这一转移灶高异质性的结果也在纪念斯隆-凯特琳癌症中心发表于2022年Cell期刊的一篇包含两万五千肿瘤样本非配对的跨癌种工作中的得到了印证(肝癌是少数转移灶异质性接近甚至超过原发灶的癌种)。
CellPress:
本研究中致癌通路Wnt激活的肿瘤亚克隆在转移中不被选择似乎有悖于已有大部分文献中的结果,您如何解释本研究和其他研究结果不一致的之处?
张力烨研究员:
确实,这个结果我们最初拿到也很难相信。但是后续一系列的数据分析和功能实验让我们理解了这个看似矛盾的结果。首先Wnt突变肿瘤呈现出冷肿瘤的特征这一点已经是在多个癌种中发现的具有跨癌种较为广泛适用的结果。但是之前的研究往往是单独评估肿瘤细胞的转移能力,在我们自己的体外实验我们也得到了和传统其他报道中一致的Wnt突变肿瘤具有转移能力更强的结果。但关键点在于Wnt野生型肿瘤亚克隆具有更强的招募免疫和成纤维细胞,并构建炎性免疫微环境的能力,在我们的体外实验加入了成纤维细胞这个因素之后,Wnt野生型肿瘤细胞反而表现出了相比于Wnt突变型肿瘤细胞更强的迁移能力。简单来说肝癌Wnt野生型肿瘤亚克隆有更强的团队作战能力,而Wnt突变型亚克隆具有更强的单兵作战能力。所以我们的结果其实是与当前文献的结果并不矛盾的。
这里我需要强调,我们这里提到的Wnt突变和野生型的亚克隆在肿瘤转移选择中是在其他突变谱基本一致的前提下比较。并不能完全直接推广到分别具有Wnt野生型和Wnt突变型的不同肿瘤之间。此外,是否具有Wnt突变亚克隆相较于Wnt野生型亚克隆,在其他肿瘤类型也是不被选择的还需要针对性研究进行验证。
CellPress:
本研究对于肝癌转移患者的诊疗有何提示?
孙云帆副研究员:
首先,由于目前结果提示肝癌早转移模式以及由此产生的较少的共有突变数目大大增加了获得可同时针对转移灶和原发灶肝癌的靶向治疗难度。具有远端转移的患者是否应该进行转移活检以决定治疗干预一直是一个有争议的问题。在诊断方面,这一发现强调了在可能的最早阶段对肿瘤转移灶进行基因组检测以确认潜在靶向治疗方案的重要性。此外,由于转移在早期发生,提示原发灶切除时点也许已经产生了远端器官无法检测到的微小转移灶的定植。这提示可切除肝癌患者早期开始新辅助治疗可能会减缓肿瘤进展并防止癌细胞的进一步扩散,而术后辅助治疗可能有助于根除微小残留病灶。
其次,我们发现了一组可以在肝癌原发灶用于预测转移风险的拷贝数变异组合,后续需要有更大的数据来印证这个转移预测模型识别高转移风险患者的可靠性。
最后,我们发现Wnt野生型原发肝癌细胞所处的微环境“热”且“耗竭”,显著富集肿瘤相关成纤维细胞,为Wnt野生型肝癌细胞向其他器官播散提供外部动力,因此靶向肿瘤相关成纤维细胞有望成为预防肝癌远处转移的治疗新策略。而Wnt野生型的肝癌转移中富集免疫抑制的HLA-E高表达的B细胞,提示我们针对这一类转移灶除了传统的免疫检查点治疗还可以考虑针对HLA-E:CD94-NKG2A的免疫检查点药物。

相关论文信息
论文原文刊载于Cell Press细胞出版社
旗下期刊Cancer Cell上
原标题:《樊嘉院士团队Cancer Cell:国际首次绘制了肝癌转移的时空多组学演化图谱 | Cell Press对话科学家》

