5月6日,北京大学第三医院魏蕊、洪天配共同通讯在期刊《Molecular Cancer》上在线发表题为“Positive feedback regulation between glycolysis and histone lactylation drives oncogenesis in pancreatic ductal adenocarcinoma”的研究论文,研究结果表明,糖酵解-H3K18la-TTK/BUB1B正反馈回路加剧了PDAC的功能障碍。这些发现为乳酸代谢重编程和表观遗传调控之间提供了新的探索和显著的相互关系,这可能为PDAC治疗中的新型乳酰化治疗策略铺平道路。

https://molecular-cancer.biomedcentral.com/articles/10.1186/s12943-024-02008-9
研究背景
01
胰腺癌是一种高度侵袭性的消化系统肿瘤,是人类最致命的恶性肿瘤,5年总生存率较低,其中胰腺导管腺癌(PDAC)占80%以上。尽管在过去十年中试图改善其治疗,但PDAC的死亡率并没有显著下降。因此,必须更清晰地了解PDAC的生长和转移机制,寻找潜在的治疗靶点和新的生物标志物来预测PDAC的预后。
除了致癌基因KRAS、肿瘤抑制基因SMAD4和TP53等PDAC驱动基因突变外,大量研究表明PDAC侵袭性肿瘤生物学与代谢物和表观遗传重布线密切相关。PDAC细胞利用“代谢重编程”来支持恶性行为,如快速增殖、侵袭和一些细胞过程。代谢物是细胞代谢的中间产物,由各种酶催化,通过相应的蛋白质翻译后修饰。越来越多的代谢物被报道参与肿瘤发生过程中多种信号通路的调控。其中,乳酸是一种丰富的肿瘤代谢物,是糖酵解的最终产物,在Warburg效应(有氧糖酵解)过程中为三羧酸循环提供燃料。糖酵解增强和乳酸积累是各种类型癌症的共同特征。然而,代谢重编程如何重塑表观遗传改变,特别是PDAC中的乳酰化,仍不清楚。
组蛋白参与调节各种生理功能,组蛋白的翻译后修饰(如乙酰化、琥珀酰化)在疾病的发展中起着重要作用。核心组蛋白上的乳酸衍生乳酰化已被多个研究小组证实为一种新型的组蛋白标记。 到目前为止,已经鉴定出28个组蛋白乳酰化位点,包括组蛋白H3赖氨酸4和组蛋白H3赖氨酸18(H3K18)等。组蛋白通过影响下游基因的表达和激活来发挥生物学效应。组蛋白的乳酰化优先影响参与碳水化合物、氨基酸、脂质和核苷酸代谢等基本代谢途径的酶。然而,涉及组蛋白乳酰化治疗以克服和改变PDAC分子景观的策略尚未实现。因此,在PDAC病理学中更好地了解组蛋白乳酰化仍需要进一步研究。
研究发现
02
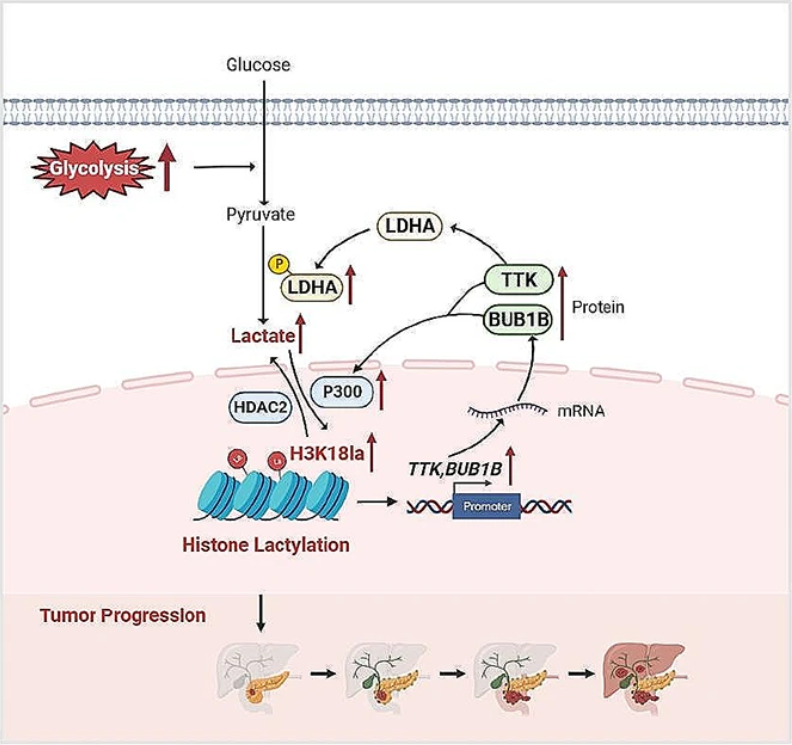
PDAC肿瘤微环境中的乳酸积累在体内和体外驱动组蛋白乳酰化,与肿瘤发生和不良临床结果密切相关。机制上,PDAC中糖酵解的增强导致乳酸产生和H3K18la增加,从而促进TTK蛋白激酶(TTK)和BUB1有丝分裂检查点丝氨酸/苏氨酸激酶B(BUB1B)的转录。TTK和BUB1B上调了P300;TTK激活乳酸脱氢酶A(LDHA),上调乳酸生成,促进组蛋白乳酰化,从而形成糖化-H3K18la-TTK/BUB1B的反馈回路。作为原理证明,研究结果首次揭示了组蛋白乳酰化,特别是H3K18la在PDAC中的新作用,而糖酵解-H3K18la-TTK/BUB1B正反馈回路的破坏可能是PDAC补充治疗的潜在治疗方法。
研究结论
03
综上所述,研究结果表明,糖酵解-H3K18la-TTK/BUB1B正反馈回路加剧了PDAC的功能障碍。这些发现为乳酸代谢重编程和表观遗传调控之间提供了新的探索和显著的相互关系,这可能为PDAC治疗中的新型乳酰化治疗策略铺平道路。(转化医学网360zhyx.com)
参考资料:
https://molecular-cancer.biomedcentral.com/articles/10.1186/s12943-024-02008-9
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。

